本日は有機金属試薬について講義していきます!
目次の【発展】はウォーレン有機化学(以下ウォーレン)には詳しい記述があるものボルハルト・ショア―有機化学(以下ボルハルト・ショア―)では記述がないかコラムで乗っているか問題には関係ないところなので定期テスト対策だけのボルハルト・ショア―を使っている学部生はスキップでOKです!(またColumnもへ―そうなんだくらいでいいと思います。)ウォーレンを使っている方以上の知識を持っている方なら挑戦してみましょう!
【深淵】はどちらの教科書にも記載のない内容で、更に有機化学を知りたいという皆さんは読んでみてください!
0.有機金属反応剤の原理と有用性
まず、なぜ有機金属反応剤は有用なのでしょうか?それは炭素の求核性にあります。電気陰性度というものを大学ないし高校化学では多くの人が習っていると思います。ここではPaulingの電気陰性度を基に考えてみましょう。以下がPaulingの電気陰性度の抜粋です。
| Li | Mg | C | N | O | Cl | F |
| 1.0 | 1.3 | 2.5 | 3.0 | 3.5 | 3.2 | 4.0 |
普通有機化学で炭素と結合するものと言えばN(窒素)やO(酸素)、X(ハロゲン)などが挙げられます。
ここでこれらと炭素の電気陰性度を比較すると炭素は基本的に小さいため電子を引っ張る力が小さいです。よって電子は引っ張られ結合は分極し炭素はδ+となります。しかし、今回の有機金属反応剤の炭素ー金属結合については炭素のほうが電気陰性度が大きく同様な理論の基では炭素上はδ-となります!(これはハロゲン化アルキル時の分極とは逆の分極をするという点から逆分極と言われる。)有機化学はざっくりいうと+と-を帯びた原子同士が結合するのでカルボニル基への攻撃など限定的ではありますがC-C結合(すなわち、炭素同士を結び付ける)が可能になります!
1.有機金属反応剤の作り方
1-1.Grignard反応剤
有機化学を学ぶものならだれもが聞いたことのあるGrignard反応剤。これはエーテル系の溶媒中で金属マグネシウムをハロゲン化アルキル(ボルハルト・ショア―ではハロアルカンと表現されていますね)と反応させることで調製できます。以下に反応例を示します。
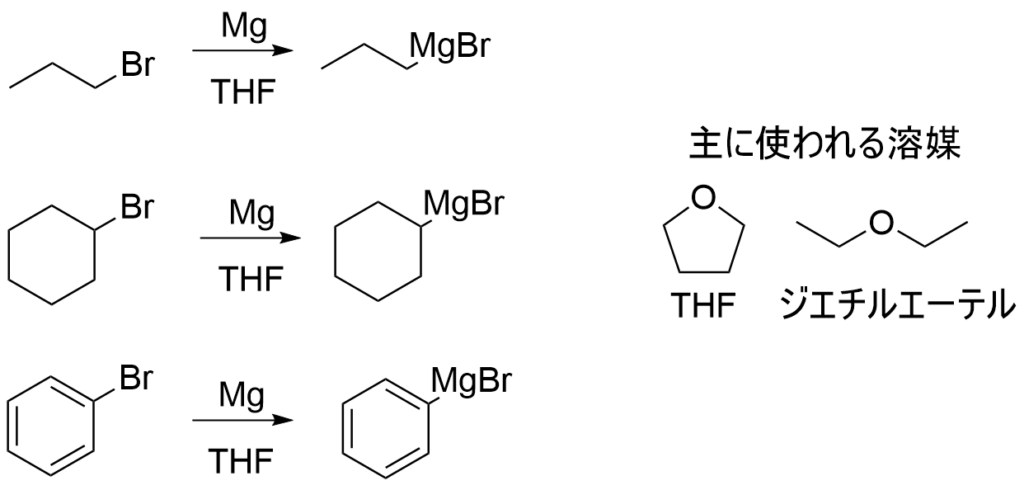
ここで溶媒としてTHF(テトラヒドロフラン)使用しています。この溶媒はエーテルのため反応性が非常に低く、禁水反応にはもってこいの溶媒です!グリニャール反応剤を作る際の溶媒としては超頻出です!(有機金属作る反応ってなったら溶媒にとりあえず書いておけば減点はされないでしょう笑)
1-2.有機リチウム化合物
Grignard反応剤とほとんど同じです。違うところとしては、金属Liが2当量必要になり有機リチウム化合物と同時にハロゲン化リチウムが1当量生成する点です。以下に反応例を書きます。
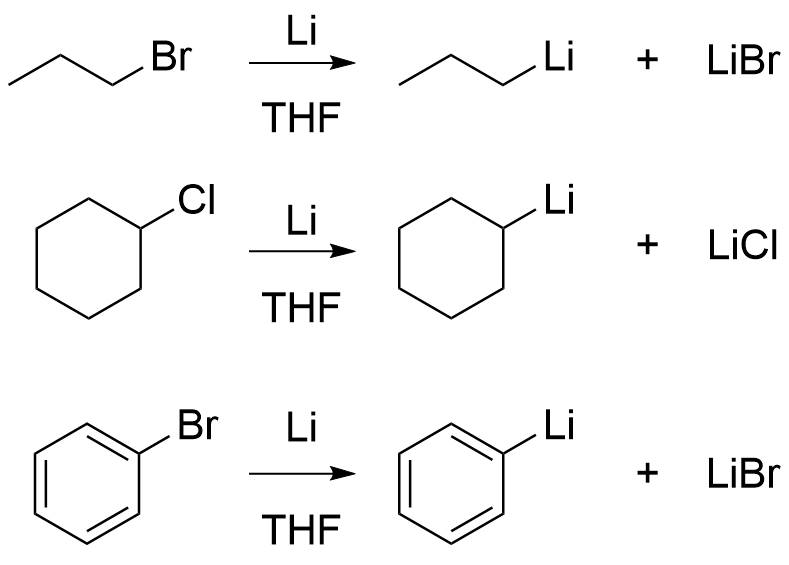
1-3.これらの反応の促進理由【発展】
ここからはこの金属の挿入反応について議論していきます。
ここではGrignard反応剤を例にとると、炭素ーハロゲン結合に対してMgが挿入する形での反応となっています。ここで反応前後のMgについて酸化数が0→2になっていることがわかります。したがってこの反応は酸化的挿入や酸化的付加と言います。この反応が促進するのはMg(0)よりもMg(Ⅱ)のほうが安定であるためです。(Liも同様にLi(0)よりもLi(Ⅰのほうが安定)
1-Column.Grignard反応剤の真の姿
Grignard反応剤は溶媒中でどうなっているでしょうか。
反応式中ではR-MgBrのように表記するのが一般的ですが真の構造ではないと言われています。この構造だと金属イオンが非常に電子不足な状態です。ここでMg(Ⅱ)は四面体の構造をとったときに安定であるために溶媒中では以下のように溶媒のエーテル2分子が配位し、四面体錯体を作っていると考えられています。(図が汚いので類似画像が第8版ボルハルト・ショア―(上)のp388に記載がありますので参照ください🙇)
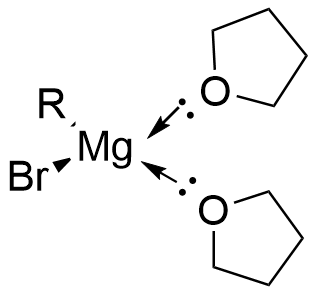
Grignard反応剤はこのような構造をしていたのですね!ちなみにGrignard反応剤はこの配位がないと生成が難しいために反応式には記載しなくていいけど重要な役割を果たしていることは知っておきましょう!
2.有機金属試薬の反応
2-1.プロトンとの反応 ~どうして水を溶媒に使ってはいけないのか~
有機金属試薬は非常に強い塩基です。よって水のように有機金属化合物をプロトン化できるものであればすぐに以下のような反応を起こして発熱的にアルカンを生じます。(例としてメチルリチウムの水との反応を挙げました。)
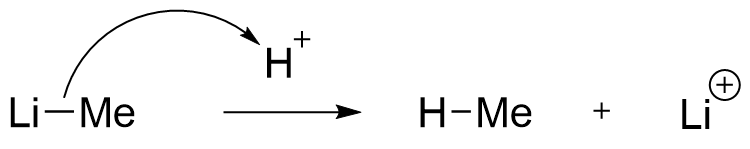
Grignard反応剤の場合でも機構は同様であり、今回ではメタンとリチウムイオンのほうが元のメチルリチウムより安定であるためにこの反応が起きます。
2-2.ハロゲン-金属交換【発展】
この反応は有機リチウム化合物がハロゲン化アルキルやハロゲン化アリールからハロゲン電子をリチウムと交換するように結合するものです。
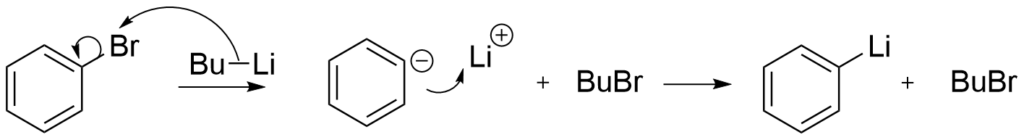
この機構のカギとなるのは酸性度とpKaです。(これらの詳しい定義などはまた解説します。)
今回はベンゼンのpKa(約43)がpKa(約50)となりベンゼンのほうが酸性であるために、フェニル錯体のほうが安定である。よってこのような反応が起こる。(pKaでピンとこない人は酸性度がアルカン<アルケン<アルキンの順になっていることを思い出そう!)
2-3.R-R’結合への応用ができない理由と根岸クロスカップリング【発展】
この反応を少し理解してきて実際に合成の練習問題に応用しようとしている人(1年前の僕です笑)はこのように考えることがあると思います。
「ハロゲン化アルキルとGrignard反応剤では炭素の分極するのが+とーだからそのまま結合して炭素鎖を増やす反応ができるのでは?」以下のような反応ですね。
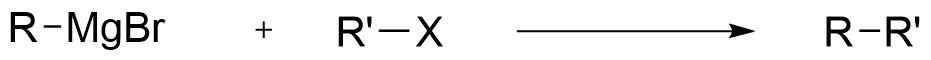
しかしこの反応はうまく進みません
これは先に述べたハロゲンー金属交換が起こってしまうためです。ボルハルト・ショア―などでは下巻のカルボニル基やカルボン酸の章あたりでHell-Volhard-Zelinsky反応を学んだ有機合成の後などに複合するとあたかも使えそうな問題がいくつかありますが罠なので気を付けましょう笑(この反応などはまた別の機会に講義します。)
ただし、これは例外が存在します。2-2でハロゲンー金属交換が起こる理由は酸性度がカギになっているということを覚えていますか?
ここで炭化水素で一番酸性度の高いアルキンのpKaはなんと約25程度です。よってアルカンと比べると非常に酸性度が強いためにアルキニル金属とハロゲン化アルキルのカップリング反応のみうまく進むことが知られています(下は反応有機リチウム化合物での反応です。)

それではR-R’のような単結合同士の炭素を伸長するようなカップリング反応はないのでしょうか?
答えとしてはあります。(しかもたくさん笑)
今回は有機金属化合物を使うときの反応として根岸クロスカップリングを紹介します。これは遷移金属を用いた有機化合物はGrignard反応剤のような普通の有機金属化合物に比べて塩基性が低く、反応が制御しやすくなるという点を用いて有機亜鉛化合物を用いた反応になります。
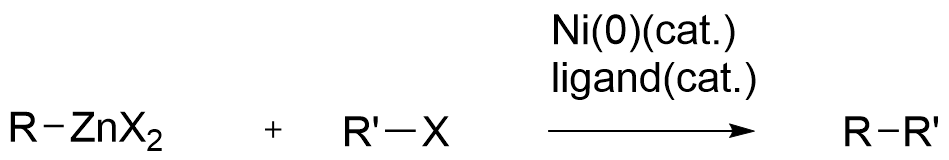
触媒はPd(0)でも可。これは反応性の低さより温和な条件で行うことができ、カルボニル基のようなGrignard反応剤には不安定な官能基にも適用できます。
この反応はまず第一段階に有機リチウム化合物やGrignard反応剤を電気陰性度の大きい金属塩で処理することにより別の有機金属化合物が生成する金属交換反応より始まります。

この反応で根岸クロスカップリングの有機亜鉛化合物を生成できる。
2-4.熊田・玉尾・コリュークロスカップリング【深淵】
Grignard反応剤を用いたようなカップリングは塩基性が高くて副反応が強く、できないと思っていましたがこんな反応があったんです!(しかもカップリング反応のパイオニアの1つ笑)
アリールハライドやアリールトリフラートとグリニャール反応剤との反応。以下のようなベンゼン環をダイレクトにつなげるビアリール化合物の合成が有名です!
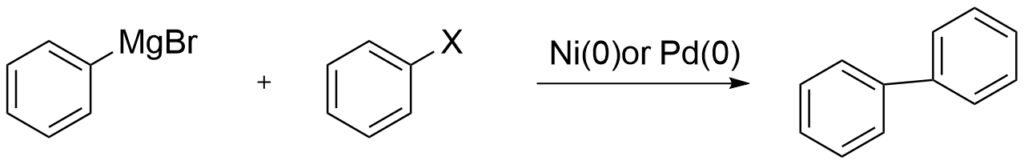
当時このようなビアリール化合物を作るのに悪戦苦闘していた時代。このカップリング反応は当時の化学者にとってまさに魔法のようなものだったのではないでしょうか!
一応注意点として有機亜鉛化合物を使った根岸クロスカップリングに対し、この反応はGrignard反応剤を使っているためにカルボニル基のような官能基に対しては副反応が起きてしまいます。
2-5.有機金属化合物のカルボニル基への攻撃【重要】
おまたせしました。ここにきてようやく定期テストの頻出内容中心となります!
有機金属化合物の反応で最も大事であるといってもいいカルボニル基への攻撃でケトンやアルデヒドと反応し酸水溶液中で処理することでアルコールを与えます。
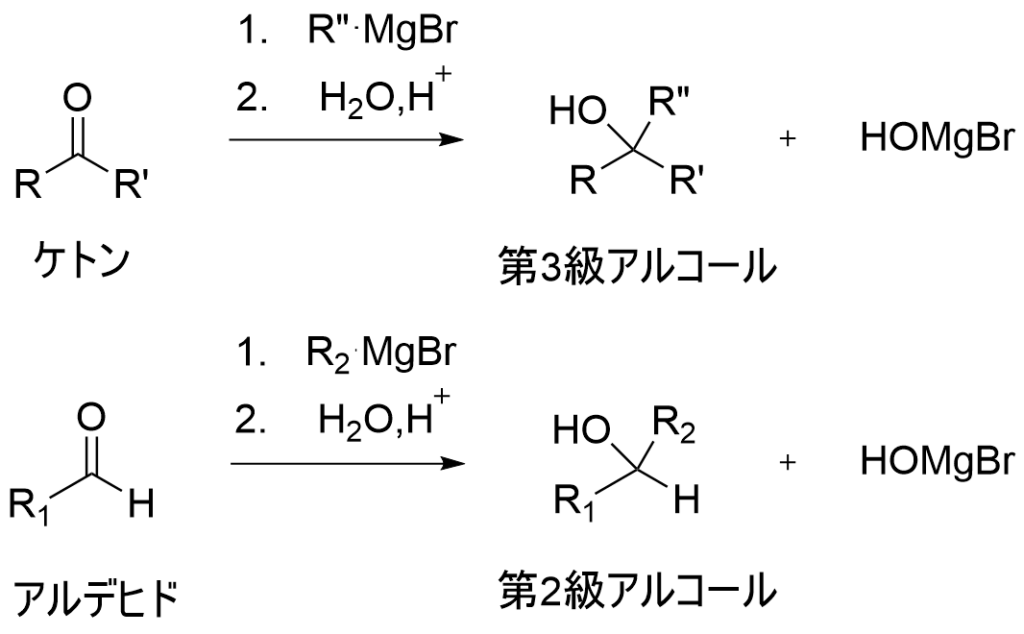
(注意!ボルハルト・ショア―には反応の際に1段階目の反応で溶媒としてジエチルエーテルやTHFを使用していることも表記していました。どちらも今回のような水がダメな反応ではよく用いられる溶媒です。定期テストなどで減点が怖い場合は入れておくと無難です。詳しくはボルハルト・ショア―上巻392ページの反応を参照ください。)
この反応は見出しの0章でも述べましたが、まず電気陰性度の観点からカルボニル基はCとOが結合しており電子はOのほうに引っ張られます。結果としてCは電子不足となりδ+を帯びます。一方Grignard反応剤はMgとCの結合よりCが電子を引っ張ることができ電子豊富な状態、すなわちδーとなります。
よって電子が欲しいδ+のCと電子を与えたい電子豊富なδーのCが結合するというのが反応のタネとなります。
この考えを基に反応機構を覚えておきましょう!以下に示しますが反応機構は手を動かすのが一番早く覚えられます。機構としては短いですし目をつぶってでも書けるくらいには仕上げましょう笑
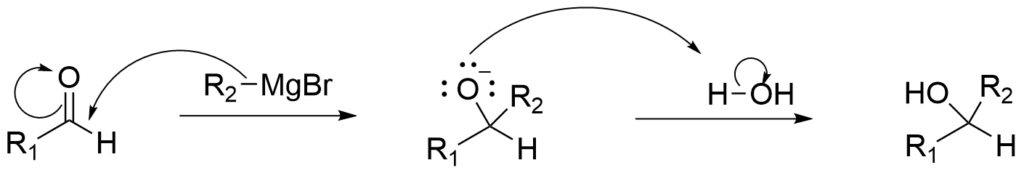
次に、このGrignard反応剤を用いて第1級アルコールを作ることはできないのか?と思うかもしれません。実は第1級アルコールはホルムアルデヒドを用いて作ることが可能です!
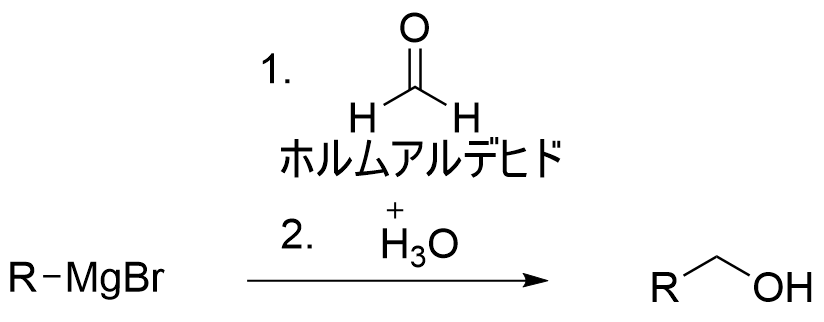
この反応はアルキル基に1炭素のユニットが付加している。この構造を保ったままい1炭素を伸長させる反応をホモログ化といい、ホモログ化ができるこの反応は大変貴重です!
【参考】ホモログ化ができるためにGrignard反応剤にホルムアルデヒドを反応させるのは非常に有用であるが、ホルムアルデヒドは通常、水和か重合体であるために、純粋な無水ホルムアルデヒドを得るためには加熱による熱分解が工程として必要になってきます。(反応式に書く必要はない)
2-6.有機金属化合物と二酸化炭素
今回はボルハルト・ショア―は下巻の19章に乗っている反応です。
有機金属化合物はその塩基性の強さからアルデヒド、ケトンのほかにも二酸化炭素にも攻撃します。(この二酸化炭素を攻撃する反応を炭酸塩化といいます。)
反応としてはGrignard反応剤や有機リチウム化合物にTHF中でドライアイス状態か、乾燥したCO2を吹き込むことによってカルボン酸塩が生じ、酸水溶液中で処理すると生成物としては炭素の1つ増えたカルボン酸が生じます。
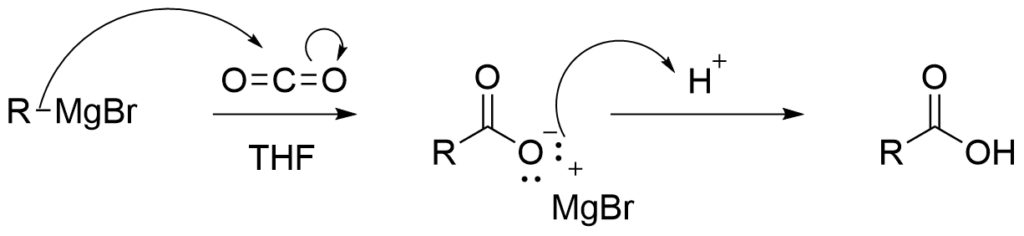
ここでは1段階目の反応はこれまで見てきたGrignard反応剤と同様に禁水であるために反応を書くときは1.CO2, THF 2.H+,H2Oと書く必要があります。
この反応は立体障害の大きなハロゲン化アルキルにおいても反応が進行できることは覚えておこう!(カルボン酸の有機合成において重要になってきます)
3.おわりに
今回は有機金属化合物の反応について基礎的な知識を見ていきました!
ボルハルト・ショア―には10ページ程度でサラッと書かれていた内容だと思うので、ウォーレンやケムステなどの情報から総合的にまとめてみるとこんなにボリューミーでありびっくりした方もいるかもしれません。
有機金属反応剤はこれからも多くの章で合成の1つとして出で来るのでここでマスターしておきましょう!
4.参考文献
・K.P.C.Vollhardt,・N.E.Schore著(古賀憲司・野依良治・村橋俊一監訳).”ボルハルト・ショア― 現代有機化学(第8版)[上]”.化学同人.2023. p386~p396.
・K.P.C.Vollhardt, N.E.Schore著(古賀憲司・野依良治・村橋俊一監訳).”ボルハルト・ショア― 現代有機化学(第8版)[下]”.化学同人.2020. p1146~1147.
・J.CLAYDEN・N.GREEVES・S.WARREN著(野依良治・奥山格・柴崎正勝・檜山爲次郎監訳).”ウォーレン有機化学(上)第2版”.東京化学同人. 2015. p183~193.
・Hiro著.”根岸クロスカップリング Negishi Cross Coupling”.Chem-Station(ケムステ)|化学ポータルサイト.2009/6/9.
根岸クロスカップリング Negishi Cross Coupling | Chem-Station (ケムステ).(参照2026/3/3).
・Hiro著.”熊田・玉尾・コリューカップリング Kumada-Tamao-Corriu Cross Coupling”.Chem-Station(ケムステ)|化学ポータルサイト.2009/6/19.
熊田・玉尾・コリューカップリング Kumada-Tamao-Corriu Cross Coupling | Chem-Station (ケムステ).(参照2026/3/3).
・諸藤達也(もろぴー)著.”熊田・玉尾・コリューカップリング / Kumada-Tamao-Corriu coupling“.有機化学論文研究所.2019/10/18.
熊田・玉尾・コリューカップリング / Kumada-Tamao-Corriu coupling | 有機化学論文研究所.(参照2026/3/3).
コメントを残す